บทความน่ารู้
FDA ให้การรับรอง Fast Track แก่ CTx001 ของ Complement Therapeutics เพื่อรักษา Geographic Atrophy (GA) – การพัฒนายาใหม่ที่อาจชะลอการสูญเสียการมองเห็นในผู้ป่วย AMD
FDA ให้การรับรอง Fast Track แก่ CTx001 ของ Complement Therapeutics เพื่อรักษา Geographic Atrophy (GA) – การพัฒนายาใหม่ที่อาจชะลอการสูญเสียการมองเห็นในผู้ป่วย AMD
การได้รับการรับรอง Fast Track จากองค์การอาหารและยาแห่งสหรัฐ (FDA) เป็นสัญญาณสำคัญที่บ่งบอกถึงศักยภาพของ CTx001 ในการเป็นยาที่อาจเปลี่ยนแปลงแนวทางการรักษา Geographic Atrophy (GA) ซึ่งเป็นรูปแบบหนึ่งของการเสื่อมสภาพจอประสาทตา (AMD) ที่ทำให้ผู้ป่วยสูญเสียการมองเห็นอย่างค่อยเป็นค่อยไป บทความนี้จะเจาะลึกถึงความหมายของ Fast Track, กลไกการทำงานของ CTx001, ผลการทดลองที่สำคัญ, และผลกระทบต่อผู้ป่วยและวงการวิจัย
ความสำคัญของ GA ใน AMD 🌍
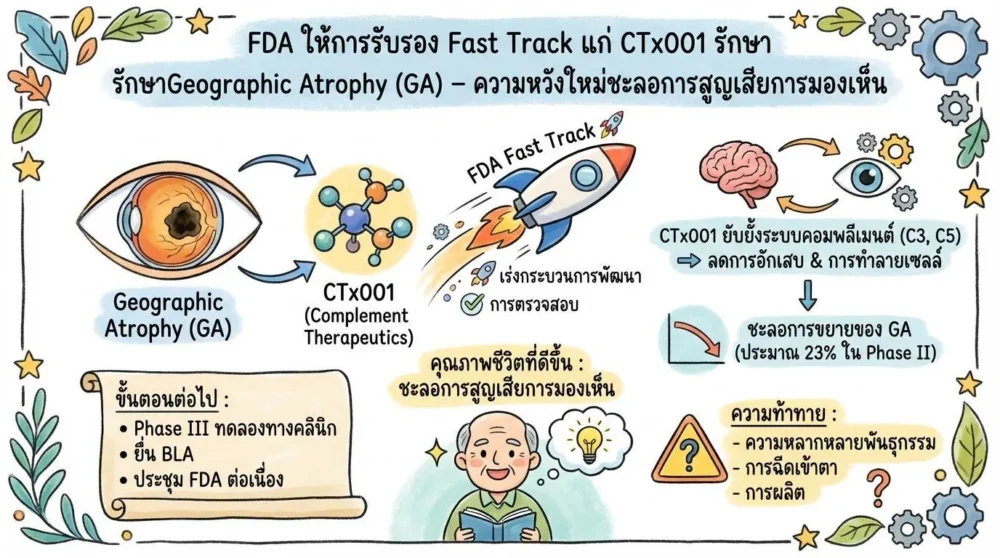
Geographic Atrophy (GA) เป็นภาวะที่เกิดจากการทำลายเซลล์ฟอตอพิก (RPE) และชั้นสภาพแสง (photoreceptors) อย่างค่อยเป็นค่อยไป ทำให้เกิด “หลุม” บนจอประสาทตาที่ขยายตัวตามเวลา ผู้ป่วย GA มักประสบกับการสูญเสียการมองเห็นศูนย์กลางและความสามารถในการอ่านหรือขับรถ ลดคุณภาพชีวิตอย่างมีนัยสำคัญ แม้ว่าอัตราการเกิด GA จะเพิ่มขึ้นกับอายุและมีความสัมพันธ์กับพันธุกรรม แต่จนถึงปัจจุบันยังไม่มีการรักษาที่สามารถหยุดหรือชะลอการดำเนินของโรคได้อย่างมีประสิทธิภาพ
FDA Fast Track คืออะไร? 🚀
Fast Track เป็นโปรแกรมของ FDA ที่ออกแบบมาเพื่อเร่งกระบวนการพัฒนายาและการตรวจสอบความปลอดภัยของยาที่ตอบสนองต่อความต้องการทางการแพทย์ที่ยังไม่มีทางเลือกที่เพียงพอ การได้รับการรับรอง Fast Track ทำให้บริษัทสามารถเข้าถึงข้อมูลเชิงลึกจาก FDA ได้เร็วขึ้น, มีการประชุมเชิงปฏิบัติกับผู้ตรวจสอบบ่อยครั้ง, และอาจได้รับการพิจารณาให้ใช้ “Accelerated Approval” หรือ “Priority Review” ในขั้นตอนต่อไป
CTx001 ของ Complement Therapeutics คืออะไร? 💊
CTx001 เป็นโมเลกุลชีวภาพที่พัฒนาขึ้นโดย Complement Therapeutics เพื่อยับยั้งการทำงานของระบบคอมพลีเมนต์ (complement system) โดยเฉพาะส่วนของ C3 และ C5 ซึ่งเป็นส่วนสำคัญที่ทำให้เกิดการอักเสบและการทำลายเซลล์ในจอประสาทตา การออกแบบให้เป็น “inhibitor” ที่เลือกเฉพาะจุดนี้ทำให้ CTx001 มีศักยภาพในการลดการทำลายของเซลล์ RPE และ photoreceptors อย่างมีเป้าหมาย
กลไกการทำงานของ CTx001 🧬
เมื่อคอมพลีเมนต์ถูกกระตุ้นในตา จะเกิดการสร้าง “membrane attack complex” (MAC) ที่ทำลายเซลล์เป้าหมาย CTx001 ทำหน้าที่ผูกกับ C3 และ C5 ทำให้การแปลงเป็น C3a, C3b, C5a, C5b ถูกยับยั้ง ผลลัพธ์คือการลดการอักเสบ, การลดการทำลายเซลล์โดย MAC, และการสร้างสภาพแวดล้อมที่เอื้อต่อการฟื้นฟูของเซลล์ RPE
ผลการทดลองระยะต้น (Phase I/II) 📊
การทดลองระยะ Phase I ที่ทำบนอาสาสมัครสุขภาพดีแสดงให้เห็นว่า CTx001 มีความปลอดภัยสูง ไม่มีอาการข้างเคียงที่รุนแรง การกระจายตัวของยาในน้ำตา (intravitreal injection) มีอัตราการคงตัวที่เหมาะสม
ใน Phase II (การทดลองบนผู้ป่วย GA) พบว่าผู้ป่วยที่ได้รับ CTx001 มีอัตราการขยายของหลุม GA ช้ากว่ากลุ่มรับสารละลายเปล่า (placebo) ประมาณ 23 % หลัง 12 เดือน การวัดความคมชัดของการมองเห็น (best-corrected visual acuity) แสดงการคงที่หรือมีการปรับปรุงเล็กน้อยในกลุ่มรักษา แม้ว่าจะยังต้องการการยืนยันในระยะยาว แต่ผลลัพธ์เหล่านี้เป็นสัญญาณที่ดีต่อการพัฒนาต่อไป
ความคาดหวังต่อการชะลอการสูญเสียการมองเห็น 👁️
หาก CTx001 สามารถยืนยันผลการชะลอการขยายของ GA ได้อย่างต่อเนื่องในระยะ Phase III ผู้ป่วยอาจได้รับ “เวลามากขึ้น” ในการทำกิจกรรมประจำวัน เช่น การอ่านหนังสือหรือการทำงานบนคอมพิวเตอร์ การชะลอการสูญเสียการมองเห็นเพียง 1–2 ปีอาจทำให้คุณภาพชีวิตของผู้ป่วยและครอบครัวดีขึ้นอย่างมีนัยสำคัญ
ผลกระทบต่อผู้ป่วยและคุณภาพชีวิต 🌟
การรักษาที่มุ่งเน้นการชะลอการเสื่อมสภาพจอประสาทตา ไม่เพียงแต่ช่วยลดภาระทางการแพทย์เท่านั้น แต่ยังลดค่าใช้จ่ายด้านการดูแลระยะยาว เช่น การใช้เครื่องช่วยมองเห็นหรือการพึ่งพาผู้ดูแล การรับรอง Fast Track ทำให้ผู้ป่วยอาจได้รับการเข้าถึงการทดลองคลินิกเร็วขึ้นและมีโอกาสรับยาที่อาจเป็น “ทางออกใหม่” ก่อนที่ยาจะเข้าสู่ตลาดทั่วไป
กระบวนการรับรองและขั้นตอนต่อไป 🗂️
หลังจากได้รับการรับรอง Fast Track, Complement Therapeutics จะต้องดำเนินการต่อไปดังนี้
- จัดทำ “Biologics License Application” (BLA) พร้อมข้อมูลจากการทดลอง Phase III
- มีการประชุมกับ FDA อย่างต่อเนื่องเพื่อปรับปรุงการออกแบบการทดลองและเก็บข้อมูลความปลอดภัยในระยะยาว
- หากได้รับ “Priority Review” จะมีการพิจารณาให้การอนุมัติภายใน 6 เดือน แทน 10 เดือนตามปกติ
ความท้าทายและความเสี่ยงในการพัฒนายาใหม่ ⚠️
แม้ว่า CTx001 จะมีศักยภาพสูง แต่ก็ยังต้องเผชิญกับอุปสรรคหลายประการ
- ความหลากหลายทางพันธุกรรมของผู้ป่วย AMD ที่อาจทำให้การตอบสนองต่อยาต่างกัน
- ความเสี่ยงของการติดเชื้อจากการฉีดสารเข้าในดวงตา (intravitreal injection) แม้จะหายาก แต่ต้องมีการเฝ้าระวังอย่างใกล้ชิด
- ความต้องการในการผลิตโมเลกุลชีวภาพที่มีคุณภาพสูงและต้นทุนการผลิตที่อาจสูง
มุมมองของผู้เชี่ยวชาญและชุมชนการวิจัย 🧑🔬
ผู้เชี่ยวชาญด้านโรคตาและนักวิจัยหลายคนให้ความเห็นว่า การมุ่งเน้นที่ระบบคอมพลีเมนต์เป็นแนวทางที่น่าสนใจ เนื่องจากระบบนี้เป็น “หัวใจ” ของการอักเสบใน GA อย่างไรก็ตาม พวกเขายังเน้นว่าการประเมินผลระยะยาวและการตรวจสอบผลข้างเคียงที่อาจเกิดขึ้นจากการยับยั้งคอมพลีเมนต์ในระบบตาเป็นสิ่งสำคัญ การทำงานร่วมกันระหว่างบริษัทเภสัชกรรม, สถาบันวิจัย, และหน่วยงานกำกับดูแลจะเป็นกุญแจสำคัญในการนำ CTx001 ไปสู่การใช้จริง
คำถามที่พบบ่อย
-
ถาม: Fast Track แตกต่างจากการอนุมัติแบบปกติอย่างไร?
ตอบ: Fast Track ช่วยเร่งกระบวนการตรวจสอบและให้การสนับสนุนจาก FDA อย่างต่อเนื่อง ทำให้บริษัทสามารถรับข้อมูลเชิงลึกและปรับปรุงการทดลองได้เร็วขึ้น ในขณะที่การอนุมัติแบบปกติอาจใช้เวลานานกว่าและไม่มีการสนับสนุนพิเศษ -
ถาม: CTx001 จะฉีดเข้าไปในดวงตาแบบใด?
ตอบ: CTx001 จะถูกฉีดโดยวิธี intravitreal injection ซึ่งเป็นการฉีดสารตรงเข้าสู่ช่องกระจกตาใต้เยื่อกระจกตา (vitreous cavity) เพื่อให้ยาสามารถเข้าถึงจอประสาทตาได้โดยตรง -
ถาม: มีผลข้างเคียงที่สำคัญของ CTx001 หรือไม่?
ตอบ: จากการทดลองระยะต้นพบว่าอาการข้างเคียงที่พบบ่อยที่สุดคืออาการบวมหรืออักเสบเล็กน้อยที่จุดฉีด ซึ่งส่วนใหญ่หายเองภายในไม่กี่วัน อย่างไรก็ตาม การติดเชื้อหรือการตอบสนองต่อยาที่รุนแรงยังคงต้องเฝ้าระวังอย่างใกล้ชิด -
ถาม: ผู้ป่วย GA ที่ได้รับการรักษาด้วย CTx001 จะต้องทำการฉีดบ่อยแค่ไหน?
ตอบ: โครงการทดลอง Phase II ใช้การฉีดทุก 12 สัปดาห์ (ประมาณ 3 เดือน) แต่อาจมีการปรับเปลี่ยนระยะเวลาตามผลการทดลองในระยะ Phase III และตามคำแนะนำของแพทย์ -
ถาม: การรับรอง Fast Track จะทำให้ยานี้มีราคาถูกลงหรือไม่?
ตอบ: การรับรอง Fast Track ไม่ได้กำหนดราคายาโดยตรง แต่การเร่งกระบวนการพัฒนาอาจลดต้นทุนการวิจัยและพัฒนาในระยะยาว ซึ่งอาจส่งผลให้ราคายาเป็นมิตรต่อผู้ป่วยมากขึ้นในที่สุด
 แอดไลน์ @187ynehr
แอดไลน์ @187ynehr