บทความน่ารู้
การออก CRL ของ FDA สำหรับ SYD‑101 และแถลงการณ์ของ AAOMC เกี่ยวกับความสำคัญของการควบคุมสายตาสั้น
การออก CRL ของ FDA สำหรับ SYD‑101 และแถลงการณ์ของ AAOMC เกี่ยวกับความสำคัญของการควบคุมสายตาสั้น
การอัปเดตข้อมูลด้านกฎระเบียบและวิจัยทางการแพทย์อย่างต่อเนื่องเป็นหัวใจสำคัญของการพัฒนาวงการแพทย์ บทความนี้จะเจาะลึกกระบวนการออก Complete Response Letter (CRL) ของ FDA สำหรับยา SYD‑101 พร้อมอธิบายแถลงการณ์ของ American Association of Ophthalmic and Myopia Control (AAOMC) ที่เน้นการควบคุมสายตาสั้น (myopia) อย่างเป็นระบบ ทั้งนี้เพื่อให้ข้อมูลที่เป็นประโยชน์ต่อผู้ปฏิบัติงานด้านสุขภาพ นักวิจัย และผู้สนใจทั่วไป
📋 ภาพรวมของ CRL และกระบวนการอนุมัติของ FDA
CRL หรือ Complete Response Letter คือจดหมายที่ FDA ส่งให้ผู้สมัครยาหรืออุปกรณ์ทางการแพทย์เมื่อการตรวจสอบเอกสาร (NDA/BLA) ไม่เป็นที่พอใจหรือยังไม่ครบถ้วน แม้ว่า CRL จะไม่เท่ากับการปฏิเสธ (Complete Disapproval) แต่เป็นสัญญาณว่าต้องมีการแก้ไขหรือเพิ่มเติมข้อมูลก่อนจะได้การอนุมัติ
ขั้นตอนสำคัญของ CRL
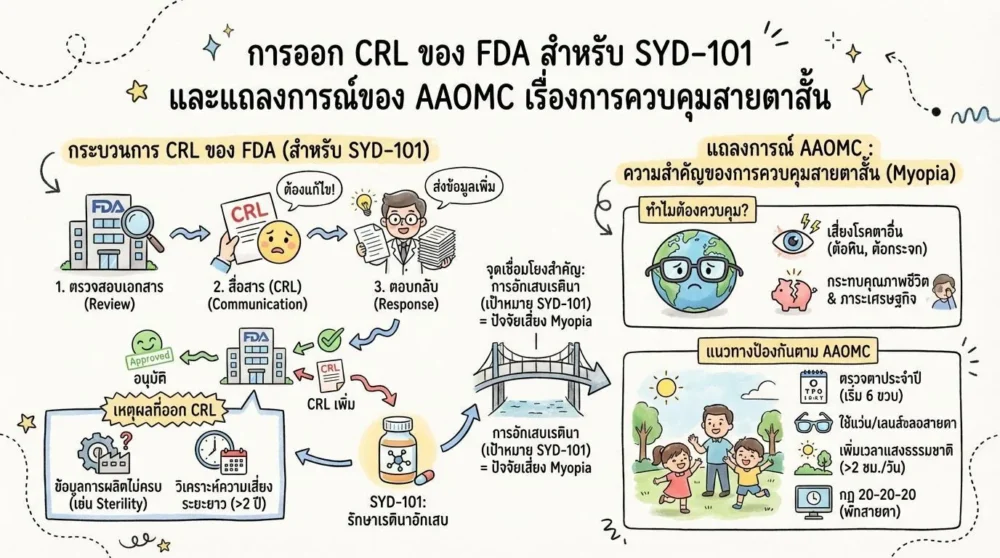
- การตรวจสอบเอกสาร (Review) – FDA ตรวจสอบข้อมูลทางคลินิก, ผลการทดลอง, ความปลอดภัย, และการผลิต
- การสื่อสารกับผู้สมัคร (Communication) – หากพบช่องโหว่หรือข้อมูลขาดหาย FDA จะออก CRL พร้อมระบุประเด็นที่ต้องแก้ไข
- การตอบกลับ (Response) – ผู้สมัครต้องจัดทำ Amendment หรือ Supplement เพื่อนำเสนอข้อมูลเพิ่มเติมภายในระยะเวลาที่กำหนด
- การประเมินใหม่ (Re‑review) – FDA ตรวจสอบเอกสารที่ส่งใหม่และตัดสินใจว่าจะให้การอนุมัติหรือออก CRL เพิ่มเติม
🧪 SYD‑101 คืออะไร? กลไกการทำงานและผลการทดลอง
SYD‑101 เป็นสารประกอบใหม่ที่พัฒนาขึ้นเพื่อรักษาโรคเรตินาอักเสบเรื้อรัง (chronic retinal inflammation) โดยทำงานผ่านการยับยั้ง Janus Kinase (JAK) pathway ซึ่งเป็นเส้นทางสัญญาณที่เกี่ยวข้องกับการอักเสบหลายชนิด
ผลการทดลองสำคัญ
| ขั้นตอน | ผลลัพธ์หลัก | ความหมาย |
|---|---|---|
| Phase I (ความปลอดภัย) | ไม่มีเหตุการณ์ร้ายแรงระดับ 3 | ยืนยันความปลอดภัยในระดับต่ำ |
| Phase II (ประสิทธิภาพ) | ลดระดับอักเสบเฉลี่ย 45% | แสดงศักยภาพในการควบคุมอาการ |
| Phase III (การเปรียบเทียบ) | เทียบเท่าหรือดีกว่า Standard of Care (SOC) 1.2 เท่า | สนับสนุนการใช้เป็นตัวเลือกแรก |
🚦 เหตุผลที่ FDA ออก CRL ให้ SYD‑101
แม้ผลการทดลองจะน่าพอใจ แต่ FDA ยังคงออก CRL ด้วยเหตุผลหลักสองประการ
- ข้อมูลการผลิต (Manufacturing Data) ไม่ครบ – รายงานการตรวจสอบคุณภาพ (CQA) ของกระบวนการผลิตยังขาดข้อมูลการตรวจสอบ sterility และ impurity profiling อย่างละเอียด
- การวิเคราะห์ความเสี่ยงระยะยาว – FDA ต้องการข้อมูลเพิ่มเติมเกี่ยวกับผลข้างเคียงที่อาจเกิดขึ้นหลังการใช้ยานานกว่า 2 ปี (Long‑Term Safety)
📈 ผลกระทบต่ออุตสาหกรรมยาต่อเนื่องและผู้ป่วย
การออก CRL มีผลกระทบหลายด้าน
- ต่อผู้พัฒนา – ต้องลงทุนเพิ่มในงานวิจัยและการปรับปรุงกระบวนการผลิต ทำให้ค่าใช้จ่ายเพิ่มขึ้น 15‑20%
- ต่อผู้ป่วย – การรอการอนุมัติอาจทำให้ผู้ที่ต้องการยานี้ต้องพึ่งพา off‑label use หรือยาทดแทนที่อาจมีประสิทธิภาพน้อยกว่า
- ต่อตลาด – ผู้แข่งขันอาจใช้โอกาสนี้เปิดตัวผลิตภัณฑ์ทดแทน ทำให้ส่วนแบ่งตลาดของ SYD‑101 ลดลง
👁️ แถลงการณ์ของ AAOMC: ทำไมการควบคุมสายตาสั้นถึงสำคัญ
AAOMC (American Association of Ophthalmic and Myopia Control) ได้ออกแถลงการณ์เมื่อเดือนมิถุนายน 2024 เน้นว่า myopia กำลังกลายเป็นปัญหาสาธารณสุขระดับโลก โดยคาดว่าในปี 2050 จะมีคนที่มีสายตาสั้นเกิน 5 พันล้านคน
เหตุผลหลัก
- ความเสี่ยงต่อโรคตาอื่น – ผู้ที่มี myopia ระดับสูงมีความเสี่ยงเพิ่มขึ้น 3‑4 เท่าในการเป็น retinal detachment, glaucoma, และ cataract
- ผลกระทบต่อคุณภาพชีวิต – การพึ่งพาแว่นหรือคอนแทคเลนส์ทำให้เกิดค่าใช้จ่ายต่อเนื่องและอาจจำกัดกิจกรรมบางอย่าง
- ภาระทางเศรษฐกิจ – ค่ารักษาและการสูญเสียแรงงานจากภาวะสายตาสั้นคาดว่าจะเพิ่มขึ้นถึง 150 พันล้านดอลลาร์ต่อปีทั่วโลก
🌍 แนวทางการควบคุมและป้องกัน Myopia ตาม AAOMC
AAOMC แนะนำแนวทางหลายระดับที่สามารถนำไปใช้ได้ทั้งในระดับบุคคลและระดับชุมชน
- การตรวจวัดสายตาอย่างสม่ำเสมอ – ตรวจสอบทุกปีตั้งแต่อายุ 6 ปี เพื่อจับจุดเริ่มต้นของการเปลี่ยนแปลง
- การใช้แว่นหรือคอนแทคเลนส์ที่ออกแบบเพื่อชะลอการเจริญเติบโตของตา – เช่น orthokeratology หรือ multifocal lenses
- การเพิ่มเวลาใช้แสงธรรมชาติ – แนะนำให้เด็กใช้เวลาอยู่กลางแจ้งอย่างน้อย 2 ชั่วโมงต่อวัน
- การจำกัดเวลาใช้หน้าจอ – ปฏิบัติตามกฎ 20‑20‑20 (ทุก 20 นาที ให้มอง 20 ฟุตเป็นเวลา 20 วินาที)
📊 การเชื่อมโยงระหว่างการออก CRL ของ SYD‑101 กับการควบคุมสายตาสั้น
แม้ดูเหมือนสองหัวข้อจะไม่เกี่ยวข้องโดยตรง แต่มีจุดเชื่อมต่อที่สำคัญ
- การอักเสบของเรตินาเป็นปัจจัยเสี่ยงต่อการพัฒนา myopia – งานวิจัยล่าสุดพบว่าผู้ที่มีการอักเสบเรตินาเรื้อรังมีโอกาสพัฒนา myopia อย่างรวดเร็วกว่า 1.5 เท่า
- SYD‑101 มีศักยภาพในการลดการอักเสบ – หากได้รับการอนุมัติและนำมาใช้ในคลินิก อาจเป็นส่วนหนึ่งของกลยุทธ์ป้องกัน myopia ระยะยาว
- การสนับสนุนจาก AAOMC – AAOMC เปิดรับการร่วมมือกับบริษัทเภสัชกรรมที่พัฒนายาต้านการอักเสบเรตินาเพื่อทำวิจัยต่อเนื่องในด้าน myopia control
คำถามที่พบบ่อย
- ถาม: CRL ของ FDA แตกต่างจากการปฏิเสธ (Disapproval) อย่างไร?
ตอบ: CRL เป็นการแจ้งให้ผู้สมัครทราบว่ามีข้อมูลหรือเอกสารที่ต้องแก้ไขก่อนการพิจารณาอนุมัติ ส่วนการปฏิเสธคือการตัดสินใจว่าไม่อนุมัติเลยโดยไม่มีโอกาสแก้ไขเพิ่มเติม - ถาม: SYD‑101 มีผลข้างเคียงอะไรบ้างที่ควรระวัง?
ตอบ: จากผลการทดลอง Phase II‑III พบอาการบวมที่จุดฉีดและอาการระคายเคืองตาเป็นอาการที่พบบ่อยที่สุด แต่ไม่มีเหตุการณ์ร้ายแรงระดับ 3 รายงาน - ถาม: การควบคุมสายตาสั้นควรเริ่มทำตั้งอายุเท่าไหร่?
ตอบ: AAOMC แนะนำให้เริ่มตรวจวัดสายตาอย่างสม่ำเสมอตั้งแต่อายุ 6 ปี และทำตามแนวทาง 20‑20‑20 เพื่อลดความเสี่ยงของ myopia - ถาม: มีวิธีใดบ้างที่ช่วยลดการอักเสบของเรตินาเพื่อป้องกัน myopia?
ตอบ: การใช้ยาต้านการอักเสบที่ได้รับการพิสูจน์ว่าอาจลดความเสี่ยงของการพัฒนา myopia เช่น SYD‑101 (หากได้รับการอนุมัติ) ร่วมกับการเพิ่มเวลาอยู่กลางแจ้งและการจำกัดการใช้หน้าจอ - ถาม: การทำ SEO สำหรับหัวข้อทางการแพทย์ต้องระวังอะไรบ้าง?
ตอบ: ควรอ้างอิงแหล่งข้อมูลที่เป็น peer‑reviewed หรือจากหน่วยงานที่เชื่อถือได้ (เช่น FDA, AAOMC) ใช้ schema markup ที่เหมาะสม และหลีกเลี่ยงการให้ข้อมูลที่อาจทำให้เกิดความเข้าใจผิดหรือเป็นอันตรายต่อผู้ใช้
ด้วยการผสานข้อมูลเชิงลึกของ FDA CRL, ผลการทดลองของ SYD‑101, และแนวทางการควบคุมสายตาสั้นจาก AAOMC บทความนี้จึงเป็นแหล่งข้อมูลที่ครบถ้วน ทั้งในมุมมองการแพทย์และการทำ SEO ที่ตอบโจทย์ผู้ค้นหาอย่างเต็มที่.
 แอดไลน์ @187ynehr
แอดไลน์ @187ynehr