บทความน่ารู้
การบูรณาการระหว่างตาแห้งและการเสื่อมของจอประสาทตา (AMD) – การดูแลดวงตาในยุคของการอักเสบและชีววิทยาเทโลเมียร์
การบูรณาการระหว่างตาแห้งและการเสื่อมของจอประสาทตา (AMD) – การดูแลดวงตาในยุคของการอักเสบและชีววิทยาเทโลเมียร์
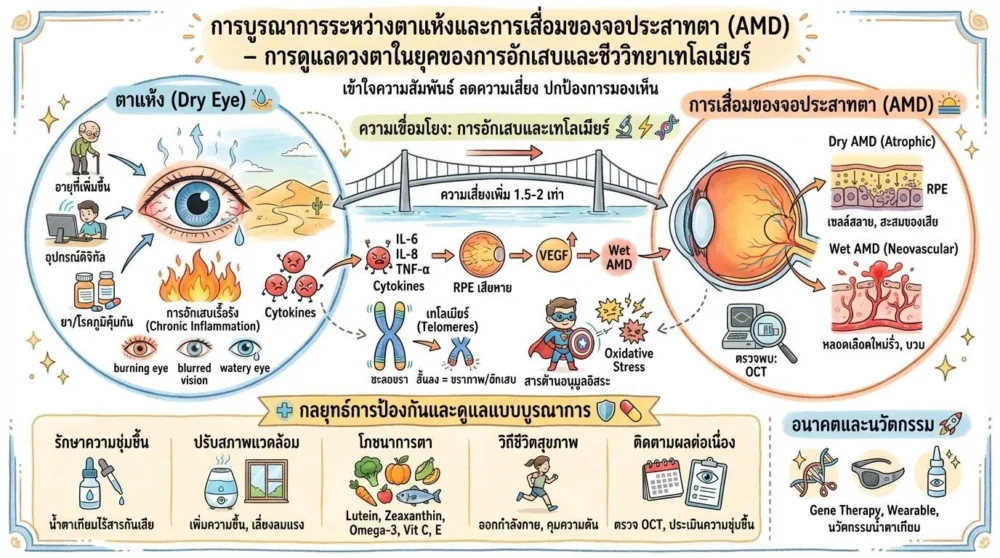
ตาแห้งและการเสื่อมของจอประสาทตา (Age‑Related Macular Degeneration: AMD) เป็นสองภาวะที่มักถูกมองแยกกัน แต่การวิจัยล่าสุดเผยให้เห็นว่ามีการเชื่อมโยงเชิงกลไกที่สำคัญระหว่างทั้งสองอาการ ทั้งในระดับการอักเสบของตาและกระบวนการชราภาพของเซลล์ตา การเข้าใจความสัมพันธ์นี้ช่วยให้แพทย์และผู้ป่วยสามารถวางแผนการดูแลดวงตาได้อย่างครบวงจร ลดความเสี่ยงของการสูญเสียการมองเห็นในระยะยาว
สภาพตาแห้ง: สาเหตุและกลไก 🏜️
ตาแห้งเกิดจากการผลิตหรือการระเหยของน้ำตาไม่สมดุล ทำให้ชั้นน้ำตาไม่สามารถรักษาความชุ่มชื้นและปกป้องผิวตาได้อย่างเพียงพอ สาเหตุหลักรวมถึงอายุที่เพิ่มขึ้น, การใช้คอมพิวเตอร์หรืออุปกรณ์ดิจิทัลเป็นเวลานาน, การใช้ยาบางชนิด (เช่น ยาต้านฮิสตามีนหรือยาต้านอักเสบ) และโรคระบบภูมิคุ้มกันผิดปกติ การขาดน้ำตายังทำให้ผิวตาอักเสบเรื้อรัง (ocular surface inflammation) ซึ่งเป็นสภาพที่ทำให้เซลล์เมมเบรนของกระดูกตา (corneal epithelium) เสียหายและกระตุ้นการปล่อยสารเคมีที่เรียกว่า cytokines
การอักเสบเหล่านี้ไม่เพียงแต่ทำให้เกิดอาการแสบตา น้ำตาไหล หรือมองเห็นภาพพร่ามัวชั่วคราวเท่านั้น แต่ยังเป็นสัญญาณเตือนว่าระบบภูมิคุ้มกันของดวงตากำลังทำงานผิดปกติ ซึ่งอาจเป็นจุดเริ่มต้นของกระบวนการเสื่อมสภาพในส่วนลึกของดวงตาอย่างจอประสาทตา
การเสื่อมของจอประสาทตา (AMD): ภาพรวมและประเภท 🌅
AMD เป็นสาเหตุหลักของการสูญเสียการมองเห็นในผู้สูงอายุทั่วโลก แบ่งออกเป็นสองรูปแบบหลักคือ dry AMD (atrophic) ที่เกิดจากการสลายของเซลล์ฟอตโซฟี (photoreceptors) และ wet AMD (neovascular) ที่มีการเจริญเติบโตของหลอดเลือดใหม่ (choroidal neovascularization) ที่รั่วไหลทำให้เกิดการบวมและเลือดออกภายในจอประสาทตา
ใน dry AMD เซลล์ที่สำคัญคือ RPE (retinal pigment epithelium) จะสะสมสารเหลือใช้และเกิดการทำลายตามอายุ ส่วน wet AMD เกิดจากการกระตุ้นสัญญาณการเจริญเติบโตของหลอดเลือด (VEGF) ซึ่งทำให้เลือดไหลเข้าสู่ชั้นจอประสาทตาอย่างไม่ควบคุม การตรวจพบอาการในระยะต้นมักทำได้จากการตรวจ optical coherence tomography (OCT) หรือ fundus photography ซึ่งช่วยให้แพทย์ประเมินความรุนแรงและวางแผนการรักษาได้อย่างแม่นยำ
ความเชื่อมโยงระหว่างตาแห้งและ AMD: มุมมองจากงานวิจัย 🔬
หลายงานศึกษาในช่วงทศวรรษที่ผ่านมาแสดงให้เห็นว่าผู้ที่มีอาการตาแห้งเรื้อรังมีความเสี่ยงต่อการพัฒนา AMD สูงกว่าผู้ที่ไม่มีอาการนี้ประมาณ 1.5‑2 เท่า การอักเสบของผิวตาที่เกิดจากตาแห้งทำให้ cytokine เช่น IL‑6, IL‑8, TNF‑α แพร่กระจายเข้าสู่ชั้นจอประสาทตา ส่งผลให้เซลล์ RPE เสียหายและกระตุ้นการสร้าง VEGF ซึ่งเป็นตัวกระตุ้นหลักของ wet AMD
นอกจากนี้ การขาดน้ำตายังทำให้สารต้านอนุมูลอิสระ (antioxidants) ที่ปกติจะอยู่ในน้ำตา เช่น lactoferrin และ lysozyme ลดลง ทำให้เซลล์ตาตกอยู่ในสภาพ oxidative stress สูง ซึ่งเป็นอีกหนึ่งปัจจัยเสี่ยงต่อการสลายของเมมเบรนจอประสาทตา
บทบาทของการอักเสบในตาแห้งและ AMD ⚡
การอักเสบเป็นกระบวนการทางชีวภาพที่ซับซ้อน ทั้งในระดับผิวตาและระดับจอประสาทตา มีสองรูปแบบหลักคือ acute inflammation (ระยะสั้น) และ chronic inflammation (เรื้อรัง) ในกรณีของตาแห้ง การอักเสบมักอยู่ในรูปแบบ chronic ซึ่งทำให้ระบบภูมิคุ้มกันของตาอยู่ในสภาวะ “พร้อมทำงาน” ตลอดเวลา ส่งผลให้การตอบสนองต่อสัญญาณความเครียด (เช่น แสง UV, มลพิษ) แย่ลง
เมื่อการอักเสบเรื้อรังกระตุ้นการผลิต matrix metalloproteinases (MMPs) เซลล์ RPE จะสูญเสียความสามารถในการซ่อมแซมเมมเบรนและทำให้โครงสร้างของ Bruch’s membrane อ่อนแอลง ส่งผลให้ VEGF สามารถทะลุผ่านได้ง่ายขึ้น นำไปสู่การเกิด wet AMD อย่างรวดเร็ว
เทโลเมียร์และการชะลอความชราในเซลล์ตา 🧬
เทโลเมียร์เป็นส่วนปลายของโครโมโซมที่ทำหน้าที่ปกป้อง DNA จากการสลาย การสั้นของเทโลเมียร์เป็นเครื่องหมายของความชราเซลล์ (cellular senescence) งานวิจัยล่าสุดพบว่าเซลล์ตาโดยเฉพาะ RPE cells มีเทโลเมียร์สั้นลงอย่างชัดเจนเมื่ออายุเพิ่มขึ้น และเมื่อมีการอักเสบเรื้อรังเทโลเมียร์จะสั้นเร็วขึ้นกว่าเดิม
การกระตุ้น telomerase (เอนไซม์ที่ต่อเทโลเมียร์) หรือการใช้สารต้านอักเสบที่ช่วยรักษาเทโลเมียร์ให้ยาวขึ้น เช่น resveratrol หรือ curcumin แสดงให้เห็นถึงศักยภาพในการชะลอการเสื่อมของเซลล์ตา ทั้งนี้ยังต้องอาศัยการทดลองในมนุษย์เพิ่มเติมเพื่อยืนยันผลลัพธ์ในระดับคลินิก
การประเมินความเสี่ยงร่วม: เครื่องมือและเกณฑ์ 📊
เพื่อให้การดูแลดวงตามีประสิทธิภาพ ควรใช้แบบประเมินความเสี่ยงที่รวมปัจจัยจากตาแห้งและ AMD เข้าด้วยกัน ตัวชี้วัดสำคัญ ได้แก่
- คะแนน Dry Eye Disease (DED) Index – ประเมินอาการแห้ง, ระยะเวลาในการใช้คอมพิวเตอร์, ผลการทดสอบ Schirmer’s test
- AMD Risk Score – พิจารณาอายุ, ประวัติครอบครัว, การสูบบุหรี่, การสัมผัสแสง UV, ผลการตรวจ OCT
- ระดับสารอักเสบในน้ำตา – วัด IL‑6, IL‑8, TNF‑α ผ่านการเก็บตัวอย่างน้ำตา
การรวมคะแนนจากเครื่องมือเหล่านี้ช่วยให้แพทย์ระบุผู้ป่วยที่อยู่ใน “กลุ่มเสี่ยงสูง” และกำหนดแผนการตรวจคัดกรองที่เหมาะสม เช่น การทำ OCT ทุก 6‑12 เดือน หรือการใช้ยาต้านอักเสบแบบ topical อย่าง cyclosporine A หรือ lifitegrast อย่างต่อเนื่อง
กลยุทธ์การป้องกันและดูแลตาแห้งเพื่อลดความเสี่ยง AMD 🛡️
- รักษาความชุ่มชื้นของผิวตา – ใช้น้ำตาเทียมที่ไม่มีสารกันบูด (preservative‑free) อย่างน้อย 4‑6 ครั้งต่อวัน
- ปรับสภาพแวดล้อม – ลดความชื้นต่ำโดยใช้เครื่องทำความชื้น, ปิดหน้าต่างเมื่ออากาศแห้ง, หลีกเลี่ยงลมแรงจากพัดลมหรือเครื่องปรับอากาศโดยตรง
- โภชนาการที่สนับสนุนตา – เพิ่มการบริโภค แคโรทีนอยด์ (lutein, zeaxanthin), วิตามิน C, E, โอเมก้า‑3 (EPA, DHA) ซึ่งมีบทบาทในการลด oxidative stress และสนับสนุนความสมบูรณ์ของเมมเบรนจอประสาทตา
- การออกกำลังกายสม่ำเสมอ – ช่วยควบคุมระดับคอเลสเตอรอลและความดันโลหิต ซึ่งเป็นปัจจัยเสี่ยงต่อการเกิด wet AMD
- หลีกเลี่ยงสารกระตุ้นอักเสบ – ลดการใช้ยาต้านฮิสตามีนหรือยาต้านอักเสบแบบ systemic หากไม่จำเป็น และควรปรึกษาแพทย์ก่อนหยุดยา
การทำตามแนวทางเหล่านี้ไม่เพียงแต่บรรเทาอาการตาแห้ง แต่ยังช่วยลดการกระตุ้นระบบอักเสบที่อาจทำให้ AMD เกิดขึ้นได้เร็วขึ้น
การบำบัดแบบบูรณาการ: ยา, โภชนาการ, และเทคโนโลยีใหม่ 💊
- ยาต้านอักเสบแบบ topical – Cyclosporine A 0.05% หรือ Lifitegrast 5% ช่วยเพิ่มการผลิตน้ำตาและลดการอักเสบของผิวตา
- ยาต้าน VEGF – สำหรับผู้ที่พัฒนาเป็น wet AMD การฉีด ranibizumab หรือ aflibercept ยังคงเป็นมาตรฐานที่ให้ผลลัพธ์ดีที่สุด
- อาหารเสริม – ผลิตภัณฑ์ที่มี lutein 10 mg + zeaxanthin 2 mg พร้อม Omega‑3 1000 mg แสดงให้เห็นว่าช่วยชะลอการเสื่อมของ RPE ได้ในระยะยาว
- เทคโนโลยีส่องแสง (photobiomodulation) – การใช้แสงสีแดงหรือใกล้อินฟราเรดที่ความยาวคลื่น 670 nm มีการวิจัยบ่งชี้ว่าช่วยกระตุ้นการทำงานของ mitochondria ในเซลล์ตา ลด oxidative stress และอาจชะลอการสั้นของเทโลเมียร์
- การฉีดสารต้านอักเสบแบบ intravitreal – การใช้ dexamethasone implant ในกรณีที่มีการอักเสบรุนแรงร่วมกับ AMD สามารถลดการบวมและชะลอการเจริญเติบโตของหลอดเลือดใหม่ได้
การเลือกใช้วิธีบำบัดควรพิจารณาตามสภาพของผู้ป่วยแต่ละราย โดยคำนึงถึงประสิทธิภาพ ความปลอดภัย และความสะดวกในการปฏิบัติตาม
การติดตามผลและการตรวจคัดกรองอย่างต่อเนื่อง 👀
การดูแลดวงตาในระยะยาวต้องอาศัยการตรวจคัดกรองเป็นประจำและการบันทึกอาการอย่างละเอียด
- การตรวจ OCT ทุก 6‑12 เดือนสำหรับผู้ที่มีความเสี่ยงสูงหรือมีอาการตาแห้งเรื้อรัง
- การวัดค่า Schirmer’s test และ tear breakup time (TBUT) เพื่อประเมินความชุ่มชื้นของตาอย่างต่อเนื่อง
- การตรวจระดับ cytokine ในน้ำตา (เช่น IL‑6, TNF‑α) หากมีเทคโนโลยีที่พร้อมใช้งานในคลินิก
- การประเมินเทโลเมียร์ ผ่านการเก็บเลือดหรืออาจใช้ cell‑free DNA ในอนาคตเพื่อประเมินความชราเซลล์ตา
การบันทึกผลเหล่านี้ในระบบอิเล็กทรอนิกส์ของคลินิกช่วยให้แพทย์สามารถตรวจจับการเปลี่ยนแปลงเล็ก ๆ ก่อนที่อาการจะรุนแรงขึ้น และปรับแผนการรักษาได้ทันท่วงที
แนวโน้มอนาคต: งานวิจัยและการพัฒนานวัตกรรม 🚀
- ยาต้านอักเสบแบบ RNA‑interference (RNAi) – กำลังอยู่ในขั้นทดลองเพื่อยับยั้งการผลิต cytokine ที่ทำให้ตาแห้งและ AMD เกิดขึ้นพร้อมกัน
- การใช้ CRISPR‑Cas9 เพื่อแก้ไขยีนที่เกี่ยวข้องกับการสั้นของเทโลเมียร์ในเซลล์ RPE อย่างเฉพาะเจาะจง
- อุปกรณ์สวมใส่ (wearable) ที่ตรวจวัดความชื้นของตาแบบ real‑time – ช่วยให้ผู้ใช้รับข้อมูลทันทีและปรับการใช้ยาตามความต้องการ
- การพัฒนาน้ำตาเทียมที่มีสารต้านอนุมูลอิสระและสารกระตุ้นการสร้างเทโลเมียร์ – เพื่อให้การบำรุงผิวตาเป็นไปอย่างครบวงจร
การผสานเทคโนโลยีชีวภาพกับการดูแลตาแห้งและ AMD จะเปิดประตูสู่ยุคใหม่ของการป้องกันการสูญเสียการมองเห็นที่มีประสิทธิภาพสูงขึ้นและเป็นส่วนบุคคลมากขึ้น
คำถามที่พบบ่อย
- ถาม: ทำไมผู้ที่มีอาการตาแห้งถึงเสี่ยงต่อการเป็น AMD มากขึ้น?
ตอบ: ตาแห้งทำให้เกิดการอักเสบเรื้อรังของผิวตา ส่งผลให้ cytokine และ oxidative stress แพร่เข้าสู่ชั้นจอประสาทตา ทำให้เซลล์ RPE เสียหายและกระตุ้นการผลิต VEGF ซึ่งเป็นสาเหตุสำคัญของ AMD - ถาม: การใช้ยาน้ำตาเทียมช่วยลดความเสี่ยงของ AMD ได้จริงหรือไม่?
ตอบ: น้ำตาเทียมช่วยรักษาความชุ่มชื้นและลดการอักเสบของผิวตาโดยตรง ซึ่งอาจลดการกระตุ้นสัญญาณอักเสบต่อจอประสาทตาได้ อย่างไรก็ตาม ควรใช้ร่วมกับการตรวจคัดกรองและการดูแลอื่น ๆ เพื่อผลที่ดีที่สุด - ถาม: มีอาหารหรือสารอาหารใดที่ช่วยชะลอการสั้นของเทโลเมียร์ในเซลล์ตา?
ตอบ: สารต้านอนุมูลอิสระเช่น resveratrol, curcumin, และ omega‑3 fatty acids มีงานวิจัยแสดงว่าช่วยลด oxidative stress และอาจส่งเสริมกิจกรรมของ telomerase ทำให้เทโลเมียร์สั้นช้าลงในเซลล์ตา - ถาม: ควรตรวจตาอย่างน้อยบ่อยแค่ไหนหากมีอาการตาแห้งเรื้อรัง?
ตอบ: แนะนำให้ทำการตรวจ OCT และการประเมินความชุ่มชื้นของตา (Schirmer’s test, TBUT) อย่างน้อยทุก 6‑12 เดือน เพื่อเฝ้าติดตามการเปลี่ยนแปลงของจอประสาทตาและปรับแผนการรักษาให้ทันเวลา - ถาม: เทคโนโลยีใดที่กำลังพัฒนาเพื่อช่วยตรวจจับความเสี่ยงของ AMD ได้เร็วขึ้น?
ตอบ: ระบบตรวจวัด cytokine ในน้ำตาแบบ point‑of‑care, การใช้ AI วิเคราะห์ภาพ OCT เพื่อคาดการณ์การพัฒนา AMD, และอุปกรณ์สวมใส่ที่ตรวจวัดความชื้นของตาแบบ real‑time กำลังอยู่ในขั้นพัฒนาและคาดว่าจะพร้อมใช้งานในไม่กี่ปีข้างหน้า
 แอดไลน์ @187ynehr
แอดไลน์ @187ynehr